- 首页
- 医院概况
- 党建动态
- 新闻中心
- 招标采购
- 科室导航
- 就医指南
- 护理园地
- 科研教学
- 专病中心
 2026/05/06
2026/05/06
 109
选择字号:
109
选择字号:小
中
大
返回列表一、资料提交要求
研究者应根据申请项目的类别,按照《临床试验项目运行管理的标准操作规程(JY-JGB-SOP-004-V2.0)》,准备临床试验研究项目相关材料(具体要求见《药物临床试验项目立项申请资料清单 AF-JGB-SOP-004-001-V2.0》)。将所有材料的电子版打包发送至中江县人民医院临床试验机构办邮箱,邮件主题格式为:项目名称+科室+PI。同时需提交纸质版材料。
二、研究项目合同
所有与外单位合作的临床试验项目,均须以医院名义签订合同(原则上使用医院模板)。申办方或CRO应将合同初稿发至临床试验机构办邮箱进行形式审查,伦理审查通过后正式签署。CRC合同在主合同签署后办理。
附件清单:
附件1:药物临床试验项目立项申请资料清单 AF-JGB-SOP-004-001-V2.0
附件2:递交信 AF-JGB-SOP-004-003
附件3:项目负责人个人简历 AF-JGB-SOP-020-001
附件4:药物临床试验立项申请表 AF-JGB-SOP-004-002
附件5:办理“人类遗传资源批件审批”的申请 AF-JGB-SOP-032-001-V2.0(如需)
附件6:关于人类遗传资源采集、保藏、国际合作、出境审批申办方承诺书 AF-JGB-SOP-032-002-V2.0(如需)
附件7:人类遗传资源承诺书签章,申请递交材料清单 AF-JGB-SOP-032-003-V2.0(如需)
附件8:人类遗传资源管理审批表 AF-JGB-SOP-032-004-V2.0(如需)
附件9:临床试验合同 AF-JGB-SOP-003-001
附件10:《临床研究协调员(CRC)技术服务合同》(三方协议)AF-JGB-SOP-003-002-V2.0
附件11:《临床研究协调员(CRC)技术服务合同》(双方协议)AF-JGB-SOP-003-003-V2.0
注:研究者提交电子版后,可致电临床试验机构办查询审核情况。审核通过后提交纸质版,机构办完成立项审核,并出具递交信回执(附件2),供研究者用于伦理备案。
临床试验机构办公室邮箱:zzxrmyygcp@163.com
临床试验机构办公室:0838-7237012
相关流程:
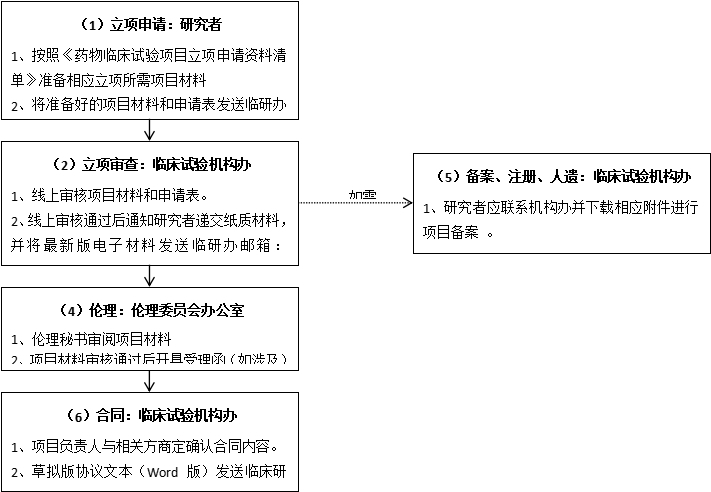
上一条
没有了下一条 2026-05-06
IIT项目资料递交指南 - 党建动态















